Le rôle des auto-anticorps IgG dans la PIDC
Chez les patients atteints de PIDC, l’activité de liaison des auto-anticorps, y compris des auto-anticorps IgG, à la gaine de myéline peut entraîner une démyélinisation, des lésions nerveuses ultérieures et l’expression de symptômes1,3,4.
Infiltration d’auto-anticorps IgG
Les lymphocytes T activés déclenchent des médiateurs inflammatoires (cytokines et chimiokines) qui franchissent la barrière hémato-nerveuse, facilitant ainsi le passage des auto-anticorps, y compris des auto-anticorps IgG1,2.
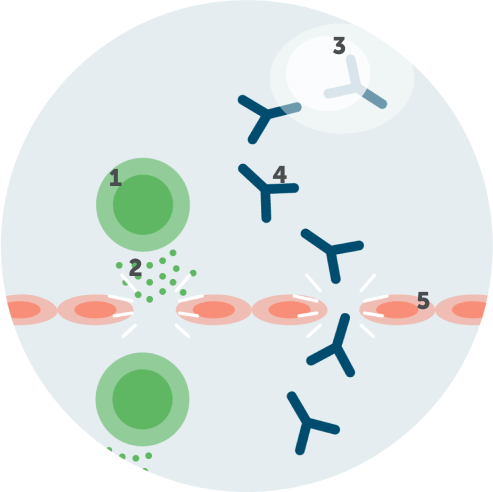
1. Lymphocyte T actif
2. Cytokines/chimiokines
3. Plasmocyte
4. Auto-anticorps IgG
5. Barrière hémato-nerveuse
Démyélinisation causée par les auto-anticorps IgG
Les auto-anticorps IgG se lient à la gaine de myéline où ils recrutent directement les macrophages ou activent la voie du complément, ce qui peut entraîner la destruction de la myéline1,2.
1. Auto-anticorps IgG
2. Macrophage
3. Récepteur Fc
4. Gaine de myéline
5. Protéines du complément
Fc = fragment cristallisable; IgG = immunoglobuline G; PIDC = polyneuropathie inflammatoire démyélinisante chronique.
Références : 1. Mathey EK et al. J Neurol Neurosurg Psychiatry. 2015;86:973–85. 2. Querol LA et al. Neurotherapeutics. 2022;19(3):864–73. 3. Dziadkowiak E et al. Int J Mol Sci. 2022;23:2–13. 4. Koike H et al. Neurol Ther. 2020;9:213–27.